今天推荐的是由苏州大学附属第二医院等单位,于2024年4月发表于Apoptosis的一篇研究论文。该研究系统揭示了SLC7A11在多发性骨髓瘤(MM)中对erastin诱导铁死亡的敏感性决定作用,全面阐述了SLC7A11表达水平与MM进展及预后的关联,深入解析了lncRNA SLC7A11-AS1通过形成RNA双链调控SLC7A11表达的分子机制,并证实了靶向SLC7A11诱导铁死亡在MM治疗中的潜在应用价值,为MM的精准治疗提供了新策略。
研究背景
多发性骨髓瘤(Multiple Myeloma, MM)是一种具有高度遗传异质性的浆细胞恶性肿瘤,尽管近年来诊疗技术取得了长足进步,但其高复发率和难以治愈的特性仍然是全球亟待解决的临床难题-。
铁死亡(Ferroptosis)是一种近年来备受关注的非凋亡性、铁依赖性氧化性细胞死亡形式,由铁介导的脂质过氧化物积累引起。与凋亡、焦亡等经典细胞死亡方式不同,铁死亡在生物学、形态学和遗传学上均表现出独特的特征-。由于癌细胞相较于正常细胞具有更高的铁需求和活性氧(ROS)水平,铁死亡在抗肿瘤治疗中展现出广阔的应用前景。
胱氨酸/谷氨酸反向转运体系统Xc⁻在维持细胞氧化还原平衡中发挥关键作用。该系统由轻链亚基SLC7A11和重链亚基SLC3A2组成,其中SLC7A11负责将胞外胱氨酸转运入胞,胱氨酸随后被还原为半胱氨酸并参与谷胱甘肽(GSH)的合成。GSH作为谷胱甘肽过氧化物酶4(GPX4)的还原底物,能够将脂质过氧化物转化为无毒的脂质醇,从而保护细胞免受铁死亡-。Erastin作为Xc⁻系统的选择性抑制剂,可通过不可逆结合并失活SLC7A11来诱导铁死亡。然而,此前有研究认为MM细胞对erastin诱导的铁死亡并不敏感。本研究对此进行了深入探索,并取得了突破性发现。
本研究发现,不同MM细胞对erastin的敏感性存在显著差异,而SLC7A11的丰度正是决定MM细胞对erastin诱导铁死亡敏感性的关键因素。高表达SLC7A11的MM细胞对erastin诱导的铁死亡更为敏感。随着浆细胞疾病谱的进展,SLC7A11表达水平逐渐升高,生存分析显示高表达SLC7A11预示着MM患者的不良预后。敲低SLC7A11表达可显著抑制MM细胞增殖并诱导铁死亡。进一步研究发现,长链非编码RNA SLC7A11-AS1是SLC7A11表达的关键调控因子,其过表达可降低SLC7A11水平并诱导MM细胞铁死亡。SLC7A11的异质性表达影响MM细胞对铁死亡的敏感性,为改善MM的临床治疗提供了理论依据。
研究内容
SLC7A11丰度决定MM细胞对erastin诱导铁死亡的敏感性
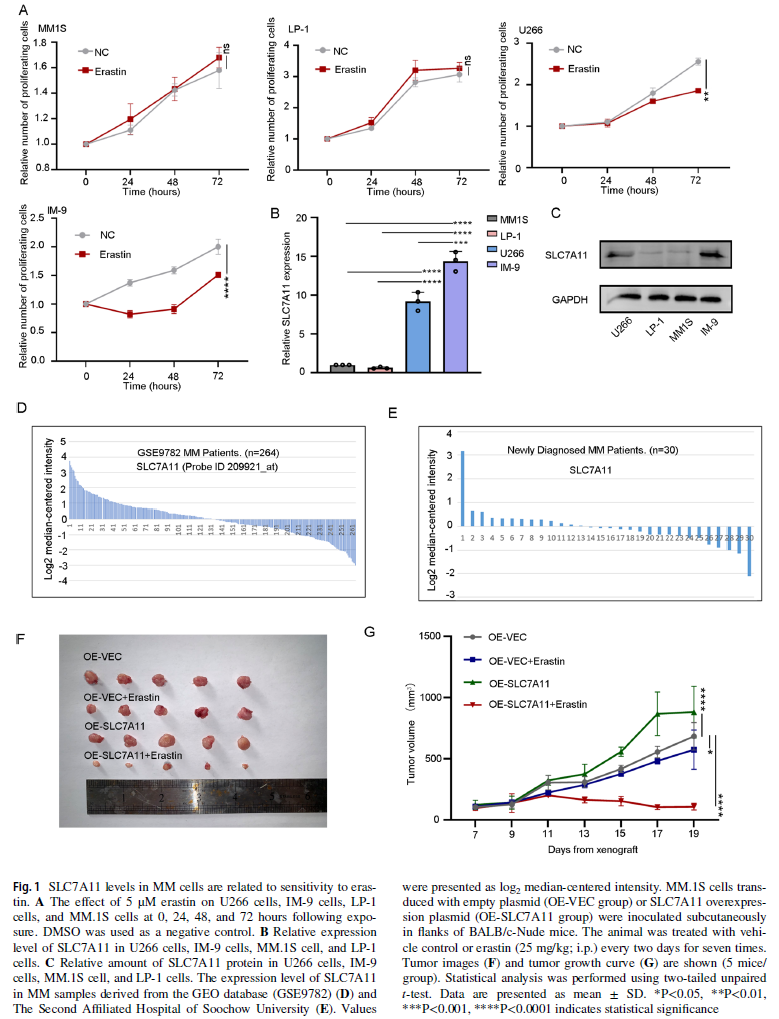
研究人员将四种人MM细胞系(U266、IM-9、LP-1和MM.1S)暴露于erastin后发现,不同细胞系对erastin的敏感性差异显著:U266和IM-9细胞的增殖受到明显抑制,而LP-1和MM.1S细胞则不受影响。值得注意的是,本研究中所有细胞系均由苏州鉴达生物科技有限公司(Genetic Testing Biotechnology)通过STR分型进行鉴定,确保了实验所用细胞系的准确性和可重复性——这是高水平论文发表的重要前提条件。
进一步检测发现,对erastin敏感的U266和IM-9细胞中SLC7A11表达水平显著高于不敏感的LP-1和MM.1S细胞。对GEO数据库(GSE9782)及临床样本的分析也证实,MM患者中SLC7A11表达水平存在巨大差异,这与MM的高度异质性特征相一致-。体内异种移植模型实验进一步证实,过表达SLC7A11可显著增强MM对erastin的敏感性。这些结果表明,SLC7A11的差异表达是MM细胞对erastin不同敏感性的根本原因。
SLC7A11高表达与MM进展及不良预后正相关
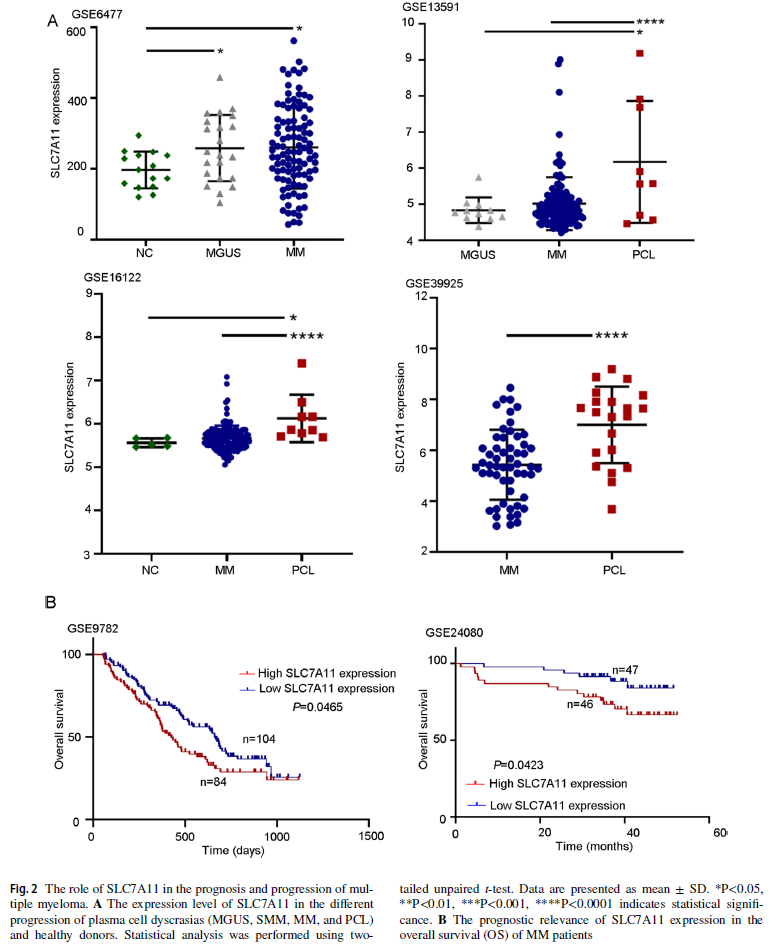
通过对GEO数据库中四个独立数据集(GSE6477、GSE13591、GSE16122、GSE39925)的分析,研究人员发现SLC7A11在MM患者CD138⁺细胞中的表达水平较健康供者显著上调,且随着浆细胞疾病谱从意义未明的单克隆丙种球蛋白病(MGUS)到冒烟型骨髓瘤(SMM)、多发性骨髓瘤(MM)直至浆细胞白血病(PCL)的进展,SLC7A11表达水平呈逐渐升高趋势。生存分析显示,高表达SLC7A11的MM患者总生存期(OS)显著较差(GSE9782和GSE24080)。这些数据表明SLC7A11在MM进展和预后中扮演着重要角色。
下调SLC7A11通过诱导铁死亡抑制MM细胞增殖
在SLC7A11高表达的U266和IM-9细胞中敲低SLC7A11表达后,细胞增殖受到显著抑制,细胞内丙二醛(MDA)和活性氧(ROS)水平升高——这两者是铁死亡的重要标志物。使用铁死亡抑制剂(铁螯合剂地拉罗司DFO或抗氧化剂Ferrostatin-1)处理后,由SLC7A11敲低引起的细胞增殖抑制及MDA、ROS升高均被显著逆转。值得注意的是,SLC7A11敲低并不诱导细胞凋亡或引起细胞周期阻滞。这些结果证实,SLC7A11下调确实通过诱导铁死亡而非其他细胞死亡方式来抑制高表达SLC7A11的MM细胞增殖。
lncRNA SLC7A11-AS1调控SLC7A11表达的分子机制
为揭示SLC7A11表达的内在调控机制,研究人员聚焦于SLC7A11邻近的长链非编码RNA,鉴定出SLC7A11的反义转录本SLC7A11-AS1。该lncRNA位于人4号染色体,与SLC7A11呈反向转录方向,在细胞核和细胞质中均有分布,且经CPC和CPAT分析证实不具备编码能力。
通过RNase保护实验,研究人员发现SLC7A11与SLC7A11-AS1之间存在276 bp的互补序列能够形成RNA双链,从而抵抗RNase的降解。相关性分析显示SLC7A11-AS1与SLC7A11表达呈负相关。敲低SLC7A11-AS1可促进MM细胞增殖并上调SLC7A11表达,同时显著延长SLC7A11 mRNA的半衰期。这些结果表明,SLC7A11-AS1通过与SLC7A11形成RNA双链,在转录后水平调控SLC7A11的稳定性。
SLC7A11-AS1通过下调SLC7A11诱导MM细胞铁死亡
生存分析显示,低表达SLC7A11-AS1的MM患者无进展生存期(PFS)较差。过表达SLC7A11-AS1后,SLC7A11表达水平下降,MM细胞增殖受到抑制,同时伴随MDA和ROS水平升高,且这种细胞死亡不涉及凋亡或细胞周期阻滞。使用铁死亡抑制剂可有效逆转SLC7A11-AS1过表达引起的细胞增殖抑制和ROS升高。共敲低实验进一步证实,SLC7A11-AS1通过调控SLC7A11表达来介导铁死亡的发生。
讨论与展望
本研究首次系统揭示了SLC7A11在多发性骨髓瘤中对erastin诱导铁死亡的敏感性决定作用,主要创新点包括:
揭示MM对erastin敏感性的异质性基础:此前研究认为MM对erastin诱导的铁死亡不敏感,但本研究发现这种不敏感性具有细胞类型依赖性,高表达SLC7A11的MM细胞反而对erastin高度敏感。这一发现挑战了既有认知,为基于铁死亡的MM精准治疗提供了重要依据。
发现SLC7A11-AS1调控铁死亡的新机制:本研究首次报道lncRNA SLC7A11-AS1通过与SLC7A11形成RNA双链来调控其稳定性,进而影响MM细胞的铁死亡敏感性。这一发现丰富了lncRNA调控铁死亡的作用机制,为非编码RNA在肿瘤治疗中的应用提供了新思路。
提出基于SLC7A11表达水平的个体化治疗策略:鉴于SLC7A11高表达与MM不良预后的正相关性,以及高表达SLC7A11的MM细胞对铁死亡诱导剂敏感的特性,针对SLC7A11高表达MM患者采用铁死亡诱导剂联合治疗可能成为一种有前景的治疗策略。
本研究同时存在一定局限性:SLC7A11-AS1调控SLC7A11的具体分子细节(如是否存在其他结合蛋白参与)仍需进一步阐明;此外,研究主要基于体外细胞实验和异种移植模型,临床转化应用还需大规模临床研究验证。
综上所述,该研究不仅深化了我们对铁死亡在多发性骨髓瘤中作用机制的理解,更为MM的精准治疗开辟了新的方向——通过靶向SLC7A11或上调SLC7A11-AS1诱导铁死亡,有望为高表达SLC7A11的MM患者带来新的治疗选择。
苏州鉴达(Genetic Testing Biotechnology, GTB)除提供细胞系STR鉴定服务外,还提供亲子鉴定业务。本公司的亲子鉴定业务包括常规的亲生血缘关系鉴定(三联体或二联体的亲权鉴定)、Y染色体鉴定、X染色体鉴定以及全同胞关系鉴定。苏州鉴达目前采用国际先进的STR检测技术,使用国际公认准确的ABI 3130 DNA遗传分析仪,亲子关系准确性高达99.99997%。如需了解更多细胞系STR鉴定及亲子鉴定的相关信息,可添加以下联系方式详询。